世の中の化学反応のほとんどが物質の表面や界面で進行しています。従って表面における分子の反応素過程を原子レベルで理解することは,触媒の解明に重要な要素であるとともに,化学の本質に関わる普遍的な課題です。本研究室では,固体表面に吸着した分子や原子を1つずつ観察して,その吸着構造や反応,ダイナミクスを調べます。原子レベルで規定された環境を用意することで,個々の分子の挙動を物理的に理解し,表面上のナノメートル領域において分子が示す特異な反応性を明らかにします。それにより化学反応における固体表面が果たす役割について,その一端を突き止めることを目標にしています。
最近の研究より
Cu(100)面上でのNOの解離反応のメカニズム
大気汚染物質の一つとして知られている一酸化窒素(NO)は、自動車の排ガスに多く含まれており現在ではその除去に三元触媒(Three-Way Catalyst)が用いられています。三元触媒はPt, Pd, Rhといった貴金属を用いた触媒で高価であることから、最近ではそれに代わって、Cuなどの地球に多く存在する金属を用いた触媒の開発を目指した研究が行われています[1]。触媒化学において反応機構を知ることは大変重要ですが、実際の触媒上で起こる反応は表面の多様性や大気圧下環境といった問題のため複雑です。そこで本研究ではCu(100)面と呼ばれる構造が規定された銅表面における超高真空(UHV)下でのNOというシンプルな系を用い、その反応機構を明らかにしました。
走査トンネル顕微鏡(STM)を用いることで分子が吸着した表面の原子分解能の像を得ることができます。図1はCu(100)面にNOを吸着させたあと測定したSTM像です。全体の大半を占めるリング状の輝点が直立して吸着したNOの単量体に、図中に2つある対になった2本の細い輝点がNOの二量体((NO)2)に対応しています。分子の種類ごとにSTMの見え方が大きく異なるのは、STM像が分子の電子状態(波動関数)を反映していることに由来しています。STM像が関わるフェルミ準位付近にはNOの2π*軌道※1が位置しています。Cu(100)面は4回対称な基板であるため(図1右上挿入図)、NOの2π*x軌道と2π*y軌道はエネルギーが縮退しています。その結果、NOの単量体はリング状として観察されます(図2上)。同様に、NOの二量体は2π*軌道のπ結合で形成される2つの軌道のうち、反結合性の軌道を反映しています(図2下)。
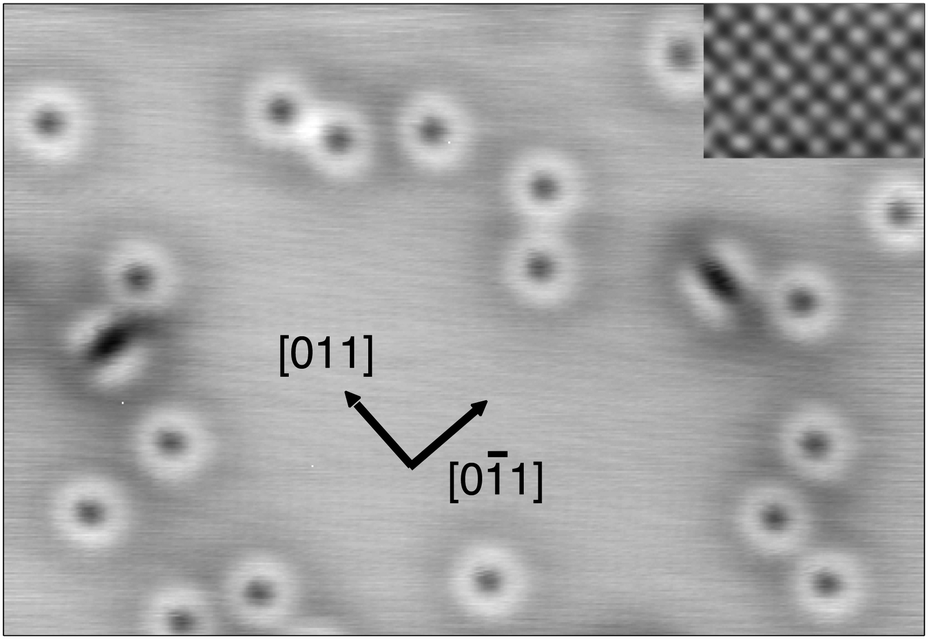
図1. Cu(100)面にNOを吸着させた後に測定したSTM像. 右上の挿入図は特殊な条件下(molecular tip)で測定して得られた基板Cu原子の配列が見えているSTM像. NOの吸着は10 K, 測定は6 Kで行った. [2]より引用.
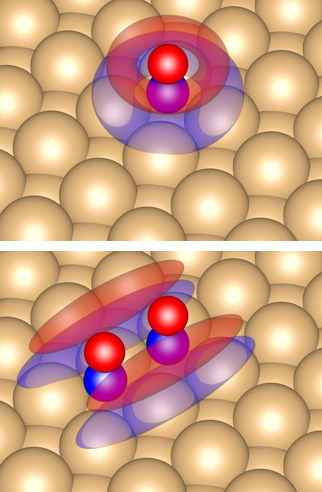
図2. Cu(100)面に吸着したNO単量体(上)と二量体(下)とそれぞれの波動関数の模式図. 赤が酸素原子を,青が窒素原子を示している.
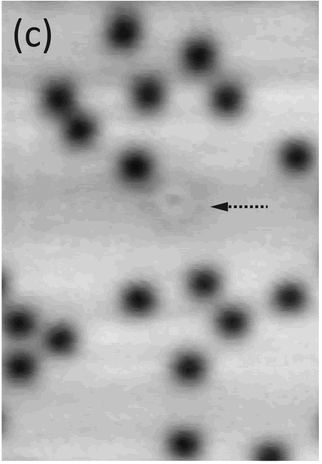
図3. 85 Kまで加熱した後のSTM像. 測定は65 Kで行った. [2]より引用.
先ほどのSTM像は6 Kで測定したものでしたが、85 Kまで表面を加熱すると表面の様子は大きく異なります(図3)。6 Kでは見られたNOの分子はほとんどなくなり、代わりに暗点状の化学種が現れています。これはNOの反応生成物であると考えられますが、STMだけでこの正体を明らかにするのは困難です。しかし電子エネルギー損失分光(EELS)による振動分光を用いることでこの問題は解決することができます。
図4は反応生成物由来のシグナルについて、NOの同位体を用いた時の振動エネルギーの変化を示しています。もともと43.8 meVに位置していたシグナル(14N16O)はNの同位体置換(15N16O)では変化しないのに対し、Oの同位体置換(14N18O)では42.5 meVにピーク位置がシフトしています。このことからこのシグナルはO原子によるものであり、STM像で見られた暗点の化学種(図3)もそれに対応することがわかりました。
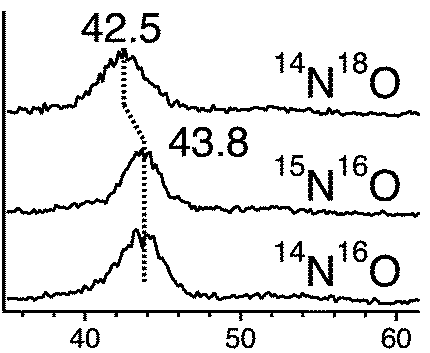
図4. NO反応生成物に対応するEELSシグナルの同位体シフト.横軸は振動のエネルギー(単位 meV)を、縦軸はその強度. [2]より引用.
NOが反応してO原子が生成される過程の詳細な機構はどのようになっているのでしょうか?そこでSTMによる単分子操作によってこれを確かめました。図5左の画像中央ににある直立したNOの二量体に電子を流し込むことで、図5中央の半円状の暗点に変わったことが観察されました。この半円状の暗点にさらに電子を流し込むと、今度は図3で見られていたものと同じ暗点、つまり酸素原子に変わりました(図5右)。一方でNOの単量体に電子を流しても反応は確認されませんでした。図5中央の半円状の暗点は、直立していたNO二量体の2π*軌道が表面との相互作用で消失しているという観点から、傾いたNO二量体であると帰属しました。以上より①NOの反応が二量体を介して起こるということ、②反応の中間体として傾いた二量体が存在すること、がわかりました。また、もう一方の反応生成物であるN2OはSTMとEELSの両方で確認できなかったことから、反応後直ちに表面から脱離したと考えられます。
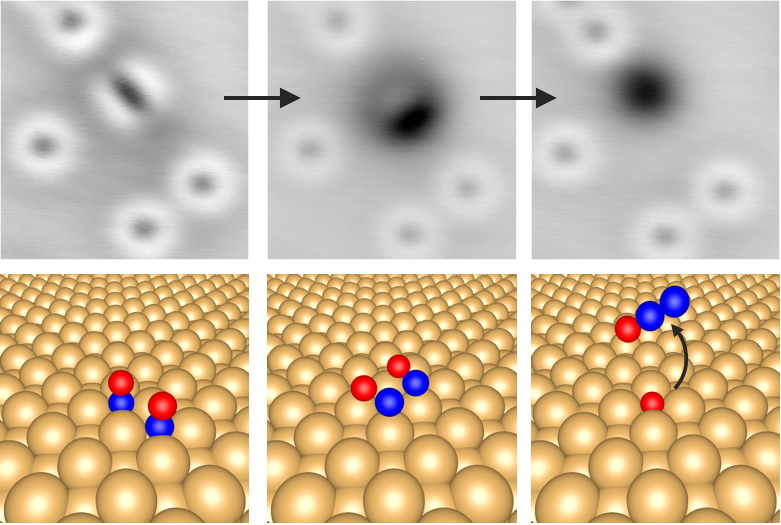
図5. 電子注入による直立したNO二量体の変化. 下はその模式図. [2]より引用, 一部改変.
反応の中間体である傾いた二量体の解離反応における役割を考えて見ましょう。直立した二量体と傾いた二量体の違いは表面との相互作用の大きさの違いにあります。酸素原子が表面の銅原子に接近しているため(π軌道と基板dバンドがより空間的に重なるため)、傾いた二量体は直立した二量体よりも表面と強く結合しています。表面との結合が強くなる分、傾いた二量体のN-O間の結合は弱くなります。これにより傾いた二量体は直立の二量体から直接解離するよりも、より低いエネルギーで解離することができます。このことは(100)面以外のCu表面でのNOの解離温度を比べることでも確認することができます。Cu(111)面やCu(110)面でのNOの解離温度はそれぞれ170 K、140 Kであると報告されている[3,4]一方で、今回Cu(100)面ではNOは~80 Kという他より低い温度で解離するということがわかりました。これはNOがCu(100)面でのみ傾いた二量体を形成するためであり、傾いた二量体が解離反応を促進する中間体として働いていることを示しています。
本文中ではNOが解離する温度(85 K)よりもう少し低い温度(64 K)では、NOは反応はしないものの表面上を拡散し、直立の二量体を一時的に形成しまた分裂する様子も示されています。以上のことからCu(100)面上のNOの解離反応は
2NO(a) → (NO)2(Upright)(a) → (NO)2(Flat)(a) → N2O(g) + O(a)
という※2、複数のステップで構成されていること、傾いた二量体が反応の中間体として働いていることがわかりました。
また本文中ではさらに、第一原理計算による反応経路の探索、傾いた二量体が反応に関わっていること、動力学計算による傾いた二量体が解離する様子、等が示されています。ぜひご覧ください。
※1 N原子とO原子それぞれの2p軌道同士のπ結合で形成される2つの分子軌道のうち、反結合性の軌道。N-O結合軸を通る節面と結合軸に垂直な節面を1つずつ持つ。
※2 (a)は表面に吸着していることを、(g)は表面から脱離していることを示す。
[1] N. Takagi et al., ACS Omega, 2019, 4 , 2596
[2] K. Kuroishi et al., Phys. Chem. Chem. Phys., 2021, 23, 16880
[3] P. Dumas et al., Surf. Sci., 1997, 371 , 200
[4] A. Shiotari et al., J. Chem. Phys., 2014, 140 , 214706

